299
PATOLOGÍA DE LAS DEMENCIAS DEGENERATIVAS QUE
AFECTAN PRIMARIAMENTE LA CORTEZA CEREBRAL
ENFERMEDAD DE ALZHEIMER (EA)
La EA es la más frecuente de las DN y su incidencia se
incrementa con la edad. La mayoría de los pacientes
presenta trastornos de memoria y desarrolla déficits
en otros dominios cognitivos, comúnmente incluyendo
apraxia, afasia y agnosia.
Macroscópicamente es llamativa la atrofia de la corteza,
la que compromete predominantemente el hipocampo,
giro parahipocampal y la amígdala temporal, estando los
lóbulos parietal y frontal menos severamente afectados.
Habitualmente el lóbulo occipital se respeta. Hay
dilatación ventricular de grado moderado, de acuerdo
al grado de atrofia cortical. También es un hallazgo
típico la despigmentación del
locus coeruleus,
con una
preservación de la pigmentación de la sustancia nigra.
Microscópicamente las placas seniles y los ovillos
neurofibrilares (ONF) han sido las lesiones características de
la EA. La pérdida sináptica también es temprana y constante.
Actualmente el diagnóstico neuropatológico de EA se basa
en la combinación de depósitos de amiloide-beta (A-beta),
de placas seniles y ONF, todos con la apropiada densidad
y distribución (1). Los criterios de diagnóstico clínico de
la EA han cambiado y actualmente descansan menos en la
demostración de demencia severa, sino en vez consideran los
estadíos más precoces de la enfermedad, cuando el deterioro
cognitivo es menor. De la misma forma ha sido necesario
desviar los criterios neuropatológicos para identificar el grado
y distribución de las lesiones asociadas al proceso patológico
subyacente pero que no están típicamente asociadas con el
estado terminal del impedimento neurológico. (1,3-5).
Depósitos A-beta:
El péptido A-beta es un fragmento de 40-42 amino
ácidos de una proteína neuronal normal llamada APP por
su sigla en inglés (proteína precursora del amiloide). Este
péptido se genera por la división secuencial del APP en
el dominio extracelular (por una proteasa conocida como
BACE), seguido por un clivaje intramembranoso (por un
complejo enzimático conocido como gama-secretasa,
que incluye la presenilina). La generación del A-beta
a partir del APP se considera crucial para el inicio de
la patogénesis de la EA, dado que mutaciones del APP
que aceleran la generación de A-beta causan las formas
familiares de EA, así como lo hacen las mutaciones de la
presenilina, las que incrementan la tasa de generación de
A-beta o la desvían hacia formas más largas de A-beta. El
descubrimiento reciente que una mutación del APP que
retrasa la proliferación de A-beta es protectora contra la
EA ha fortalecido aún más este argumento.
El A-beta, que se deposita extracelularmente, es muy
susceptible de formar diferentes tipos de agregados, lo
que morfológicamente se traduce en diferentes tipos de
depósitos o placas; los pequeños agregados (llamados
oligómeros) son actualmente los mediadores críticos
sospechosos de desencadenar la disfunción celular y
sináptica. El A-beta depositado comúnmente desencadena
una reacción local significativa, lo que pasa a constituir
la placa neurítica (Figura 2). Por otra parte se encuentran
los depósitos A-beta difusos, de aspecto convulocionado
y que no aparecen con las tinciones de rutina, pero
son inmunoreactivos con Ac anti A-beta (Figura 3). La
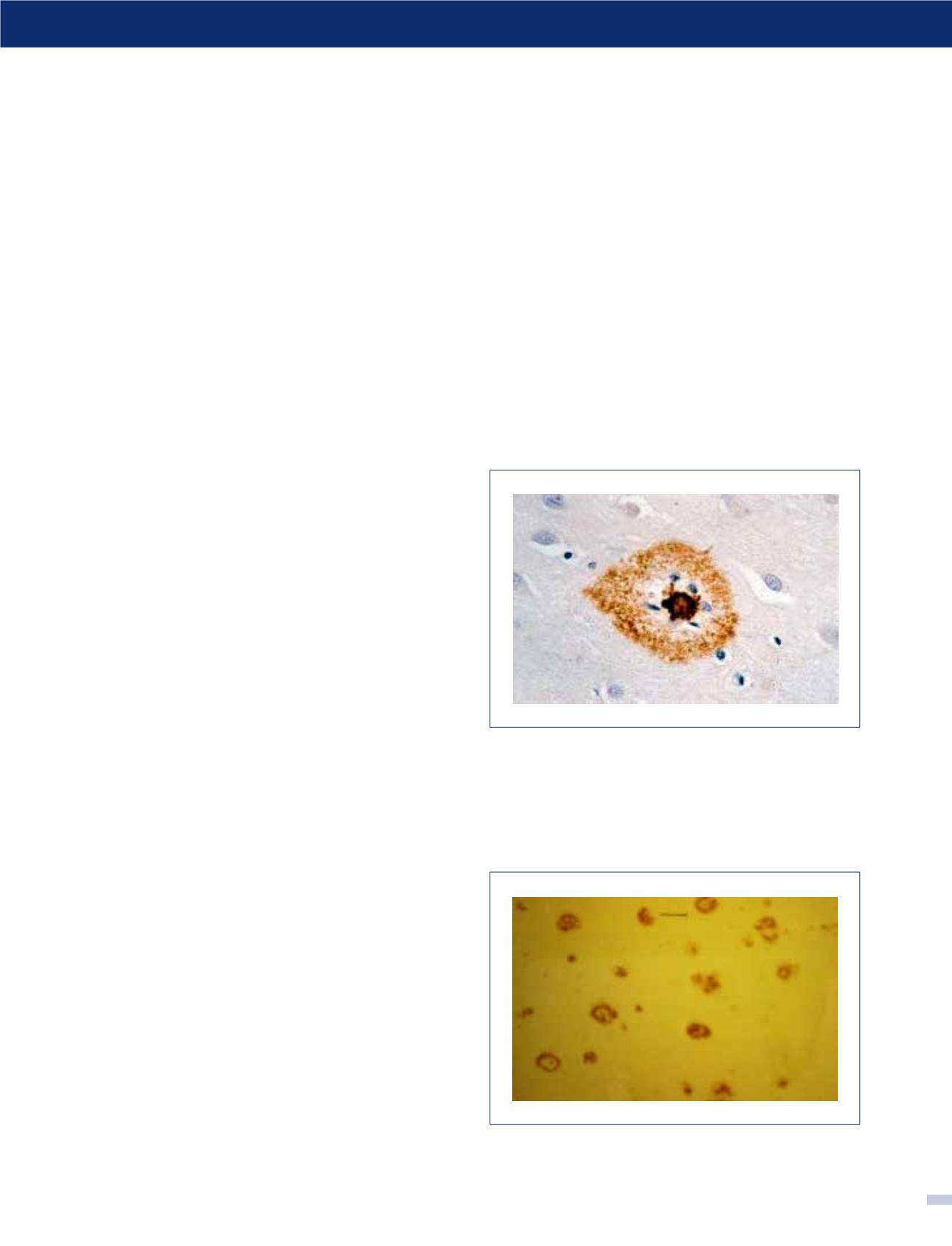
FIGURA 2. Inmunohistoquímica de amiloide beta
FIGURA 3. Inmunohistoquímica para amiloide-
beta mostrando los distintos tipos de
depósitos en la corteza cerebral en la EA
[Neuropatología de las Demencias Neurodegenerativas - Dra. Paulina Arriagada B.]
Éste se agrega en forma de depósitos insolubles en el cerebro de indi-
viduos con EA. El agregado tóxico (centro café obscuro) lleva a la
destrucción de la célula. (Foto: Hospital Universitario de Tübingen/
Mathias Jucker).
Se observan depósitos difusos, mal delimitados y otros más concentrados
en forma de placas. (Foto: colección personal).








